2023-07-03 17:20
作者 卢佳玥

京港感染论坛
多学科合作,构建诊断管理体系
![]()

从复杂样本如血液、尿液、废水等中鉴定出病原菌对于感染性疾病的诊断和治疗有着极为重要的意义。表面增强的拉曼光谱(SERS)和机器学习能鉴别多种病原菌,但要从复杂的液体样本中准确鉴定病原菌仍然极具挑战性。
近日,美国斯坦福大学的Fareeha Safir等人在《Nano Letters》杂志上发表了一篇题为《Combining Acoustic Bioprinting with AI-Assisted Raman Spectroscopy for High-Throughput Identification of Bacteria in Blood》的论文,开发了一种声学生物打印联合SERS和机器学习实现对复杂液体样本中的病原菌检测的新方法。
原文链接
https://pubs.acs.org/doi/10.1021/acs.nanolett.2c03015
可靠地检测和鉴定微生物对于临床诊断、环境监测、食品生产、生物防御、生物制造和药物开发至关重要。体外培养可用于病原体检测,然而目前的实验室方法仅能够培养不到2%的细菌,并且该过程耗时,通常需要几小时到数天的时间。
拉曼光谱是一种无标记的振动光谱技术,不同菌株具有独特的分子结构,会形成特异的拉曼指纹图谱。分析这些拉曼指纹图谱,可实现细菌物种鉴定。拉曼技术无需其他的耗材,成本较低,且拉曼技术不会破坏样本,不受水分干扰,因此具有很高的应用前景。与等离子体或米氏共振纳米粒子结合,拉曼信号平均可以增强105-106倍。基于上述优势,拉曼技术已成功应用于基因分析、蛋白质检测甚至是单分子检测,最近的研究也显示了拉曼在细胞鉴定方面包括细菌鉴定、免疫分析和体内活检等领域有一定的应用。
要将拉曼光谱进一步推广到临床检测领域,它必须与简便的样品制备方法相结合。声学液滴喷射(ADE)是有前景的生物样品液滴生成平台之一。在ADE中,超声波聚焦在流体-空气界面,产生辐射压力,从表面喷射液滴。ADE液滴的大小、速度和方向性完全由声波控制,无需物理喷嘴。ADE能够高通量生成液滴,处理流体的速率高达25000液滴/秒。此外,该平台依赖声波,使得这些波可以通过匹配的耦合介质传播,声能损失最小,同时避免样品和换能器之间的任何直接接触,消除交叉样本污染并保持无菌状态。
Fareeha Safir等人通过AED生物打印将样本数字化为单细胞或少数细胞液滴,然后使用拉曼光谱快速检测每个液滴,最后使用机器学习对结果进行分类,达到非培养检测复杂多细胞样本中病原体的目的。
该团队构建了一个氧化锌147 MHz换能器,该换能器与焦距为 3.5 mm 的石英聚焦透镜相连。换能器封装在不锈钢外壳中,并安装在机加工不锈钢板上方 3.5 毫米处,该板有一个直径为 1 毫米的孔,液滴通过该孔向下喷射。在换能器和该板之间移取200 μL样品溶液,以填充换能器的3.5 mm焦距。孔径足够大以抵消任何类似喷嘴的效应,并且流体通过表面张力保持在传感器和板的适当位置(图1 a)。研究者在该板下方1毫米处放置了一个电动可编程xy载物台,允许进行图案弹出。通过安装在 LED 对面的频闪相机监控设置,以评估液滴稳定性和喷射(图1 b)。
在试验了一系列频率和液滴直径之后(图1 c),研究者选择了147 MHz 换能器频率,液滴直径为∼15 μm或体积∼2.15 pL,以匹配细胞直径的数量级。他们发现这个体积能够打印每个液滴中细胞的液滴,同时还可以最大限度地增强金纳米棒(GNR)涂层的拉曼信号。接着该团队合成了具有960 nm纵向等离子体共振的 GNR,选择与785 nm 的激发波长一起以最小化背景荧光。合成的 GNR 离激光足够近,以被激光激发,但红移足够大,可以最大限度地减少入射光和拉曼散射光的竞争性消光(图1 d)。
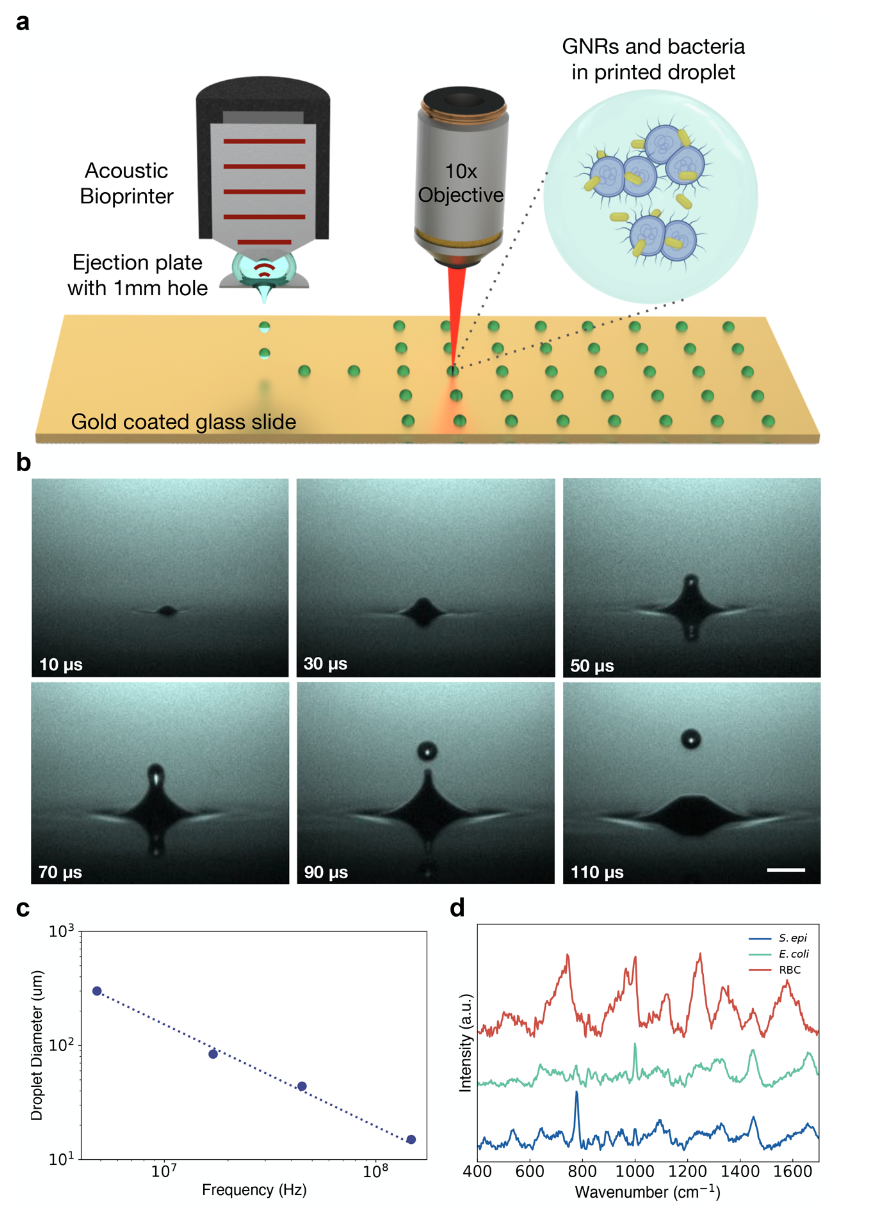
图1.(a)声学打印平台和共聚焦拉曼装置示意图。含有细菌(紫色)和纳米棒(金色)的液滴悬浮在EDTA溶液中,声学打印到涂有200nm金的玻璃载玻片上。(b)在44.75 MHz的声频和1 kHz的液滴喷射重复率下,从开放水池以 ~3.5 m/s的速度向上喷射液滴的时间演变频闪图像。图像以40 毫秒的曝光时间捕获,因此,每帧由40个液滴喷射组成,突出了喷射稳定性。(c)液滴直径与超声换能器共振频率的关系图。打印的液滴频率分别为4.8、17、44.75 和147 MHz,液滴直径分别为300、84、44 和15 μm,突出了声液滴喷射的可调性。(d)干燥细胞样品的拉曼光谱,包括镀金载玻片上的表皮葡萄球菌、大肠埃希菌和红细胞(RBC)。
该团队调整了传感器的声学脉冲宽度和输入功率,并确保打印机在每个样本的焦点上,能够可靠、精确地打印含有细菌和红细胞的液滴图案网格,这些网格包括有 GNR 和没有 GNR,喷出速度为1 kHz(图2 a)。他们还证实了通过打印,细菌仍然具有活性(图2 b)。

图2从细胞原液中喷射出有图案的液滴。所有的液滴都以147兆赫的频率喷射。(a)斯坦福大学标志的图案打印输出,打印的液滴含有1:1的表皮葡萄球菌和小鼠红细胞的混合物,在镀金的载玻片上。左图像显示了一张打印的照片(顶部)。(中)以100 μm比例尺绘制的树形区域顶部SEM图。(右)来自大面积打印的单排4个液滴,红色为红细胞,蓝色为表皮葡萄球菌。(b)将含有大肠杆菌的液滴打印到涂有琼脂的载玻片上,在37℃下孵育36小时,以证明打印样品的细胞活力。在每个位置放置100个液滴,以确保每个液滴包含细胞。
该研究团队首先打印了悬浮在乙二胺四乙酸(EDTA)水溶液中的小鼠红细胞样本,样本中加入有表皮葡萄球菌(S. epidermidis)、大肠埃希菌(E. coli)以及GNR(图3 a)。图3 b显示了含有表皮葡萄球菌和GNR液滴的放大 SEM ,证明细胞大量涂有 GNR。具有GNR的每个细胞样本的 100 个液滴的归一化平均信号和没有GNR的每个样本的15个液滴的平均信号显示在图3 c,每个液滴的光谱采集时间为 15 秒。对从统一细胞类型和混合打印的样本进行机器学习,以识别液滴成分。
该团队通过优化印刷参数、细胞到纳米棒、缓冲溶液和底物的浓度,实现跨细胞的高拉曼信号获取以及每个液滴中细胞类型的正确识别(图3 a-d,图4 a-c)。该技术在单细胞系印迹实现 ≥ 99% 的细胞分类准确度,从混合病原体样本中获得了 ≥ 87% 的细胞分类准确度,并使用液滴的扫描电子显微镜图像进行验证,以确认特定细胞的存在(图3 e,图4 c)。此外,研究者通过波数重要性来确定用于分类的关键光谱带,并确认这些特征对应已知细胞系中的生物学相关成分。(图4 d)。
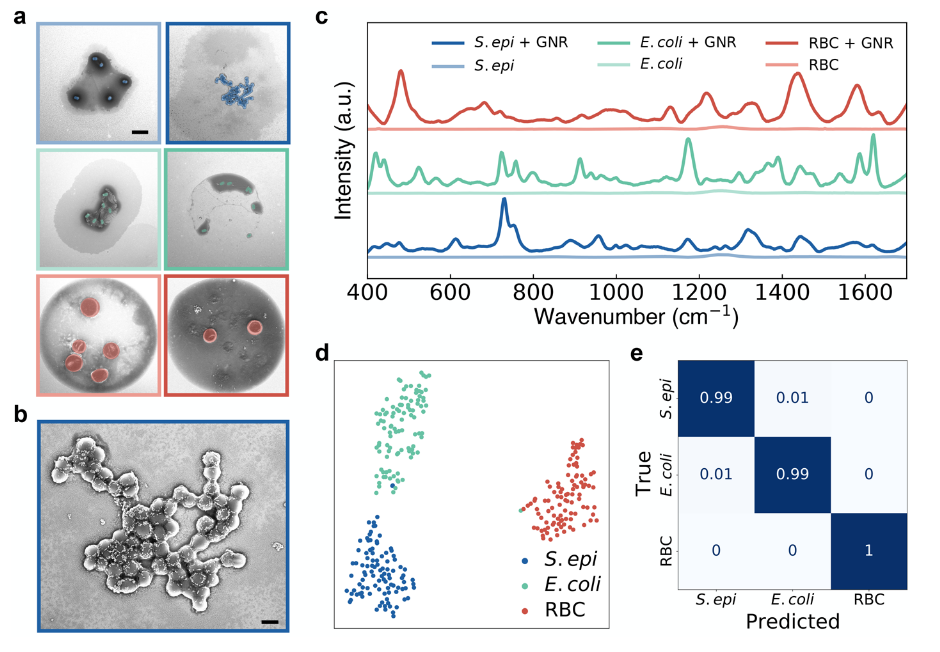
图3 含有GNR的细胞光谱鉴定。(a)SEM 显示从悬浮在EDTA溶液中的不同细胞样本打印出的单个液滴,浓度为 1e9 个细胞/mL。(b)包含涂有来自(a)的 GNR +表皮葡萄球菌的液滴的放大 SEM 。(c)100 次测量的平均 SERS 光谱,每次测量取自三个细胞系与 GNR 混合。(d)从用 GNR 打印的液滴中获取的所有300个拉曼光谱的 2 分类 t-SNE 投影。(e)使用随机森林分类器对从表皮葡萄球菌、大肠埃希菌和小鼠红细胞与 GNR 混合的单细胞系液滴收集的 300 个光谱生成归一化混淆矩阵,显示所有样本的分类准确度≥99%。该研究的算法突出显示的关键光谱带与光谱中的峰相匹配,并且这些不同的峰波数代表了文献中报道的干燥和液体的细胞系的SERS波段(图4 e)。
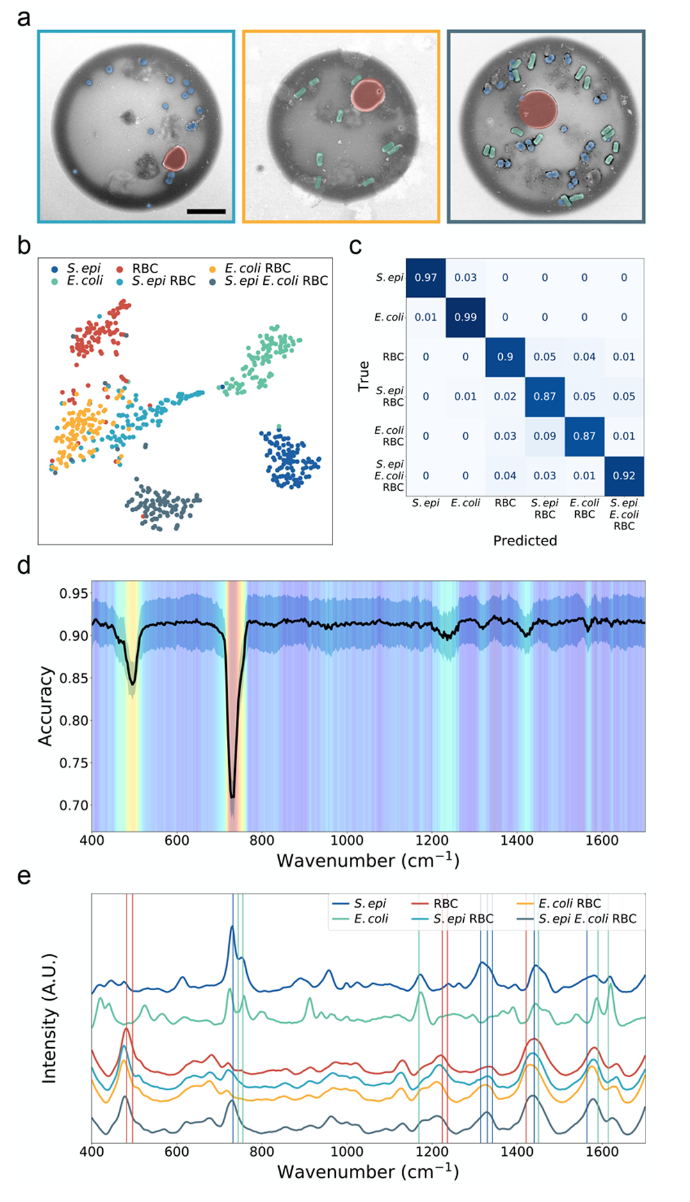
图4 (a)假色微滴SEM(从左至右)打印的微滴分别为:表皮葡萄球菌和 RBC、大肠埃希菌和 RBC 以及表皮葡萄球菌、大肠埃希菌和 RBC,这些混合物均在EDTA水溶液中稀释至1e9个细胞/mL,并与GNRs混合。(b)从三种细胞系(表皮葡萄球菌、大肠埃希菌和红细胞)和三种混合细胞系(表皮葡萄球菌和红细胞、大肠埃希菌和红细胞、表皮葡萄球菌、大肠埃希菌和红细胞)中打印的单个液滴中获得的所有600个拉曼光谱的2分类t-SNE投影。(c)使用随机森林分类器对从表皮葡萄球菌、大肠埃希菌和小鼠红细胞与 GNR 和3个细胞混合物的单细胞系液滴收集的600个光谱生成归一化混淆矩阵。(d)执行热图突出显示特征提取以确定随机森林分类中光谱波数的相对权重。(e)每100 次测量的平均 SERS 光谱图,取自三种细胞系和三种混合物与 GNR的混合。
该研究中开发的生物声打印机结合SERS纳米粒子和拉曼高光谱成像,可用于分离、计数和识别各种细胞系,实现快速、特异性和无标记的细胞分析。此外,ADE-SERS可以设计为一系列射头,以快速分离大量患者样品,单个射头也可以提供小体积的详细分析,从而最大限度地减少昂贵试剂的使用。ADE-SERS可以对低浓度样本或难培养的物种样本进行非培养细胞鉴定和监测,从而制定诊疗方案,例如循环肿瘤细胞(ctc)用于癌症筛查和监测,CD4水平用于艾滋病毒监测,结核分枝杆菌的菌株特异性鉴定。
此外,由于声学打印是无喷嘴和非接触式的,喷射器可以轻松地扫描多个不同的样品孔而不会有污染的风险。因此,ADE-SERS能够方便地实现各种患者样品或其他相关介质的多路复用。最后,鉴于本研究中底物,胶体GNR和打印平台的多功能性,这一检测系统不仅限于处理细胞,还可以改良用于检测其他生物标志物,包括小分子和蛋白质。如果加上用于标记核酸检测的表面化学方法,甚至可用于药物开发中药物样品的小批量筛查。
综上所述,该研究将SERS细胞检测与声学生物打印和机器学习相结合,为基于细胞的快速诊断研究奠定了基础,为可靠、低成本的即时诊断提供了一定的实验室数据支撑。

卢佳玥
浙江大学医学院,博士研究生
END
作者|卢佳玥(浙江大学医学院)
审校|张 嵘(浙江大学医学院附属第二医院)

