2023-09-28 17:20
作者 张丽玮

京港感染论坛
多学科合作,构建诊断管理体系

越来越多的研究者认为人类肠道共生菌会影响炎症性肠病(Inflammatory bowel diseases ,IBD)等非传染性疾病,但通过对其进行靶向抑制以缓解肠道炎症仍然是一个艰巨的挑战。以色列维茨曼研究所的学者们在《Cell》期刊上发表的一项研究,揭示了解肠道微生物组中特定型别的肺炎克雷伯菌(Klebsiella pneumoniae, Kp)与IBD之间的密切联系,并探究了利用噬菌体鸡尾酒疗法来干预肠道微生态平衡的可能性。
该文章于2022年8月4日发表在《Cell》杂志,标题为《Targeted suppression of human IBD-associated gut microbiota commensals by phage consortia for treatment of intestinal inflammation》,以色列维茨曼研究所的Sara Federici,Rafael Valde´ s-Mas,Denise Kviatcovsky和BiomX公司的Sharon Kredo-Russo为共同作者,以色列维茨曼研究所和德国癌症中心的Eran Elinav教授为通讯作者。
原文链接:https://doi.org/10.1016/j.cell.2022.07.003
![]()
▼ 1. kp在不同地区的IBD患者中富集
与健康对照组相比,克罗恩病(Crohn’s disease ,CD)和 溃疡性结肠炎(Ulcerative colitis,UC)患者的微生物丰富度较低(图1A),UC和CD患者之间以及UC或CD与健康对照组之间的粪便微生物组成分存在显著差异(图1B),法国、以色列、美国和德国的IBD患者和健康对照组相比存在显著的总体差异(图1C)。差异丰度分析表明,CD与UC患者中的5种菌种显著富集,且与疾病缓解期相比,疾病发作期的CD患者肠道中的Kp和大肠杆菌富集明显,疾病发作期的UC患者中的KP未明显降低(图1D)。
法国、以色列、美国的CD和UC患者中Kp丰度较高,德国的UC患者的Kp也有所增加(图1E-H)。根据临床症状(STAR方法)和 C反应蛋白(C-reactive protein,CRP)水平,法国、以色列、美国的IBD 患者被进一步分类为疾病发作期或缓解期(图1I)。在CD和UC患者中,与各自的缓解期患者或健康受试者相比,发作期患者之间的粪便微生物群落结构存在明显差异(图1J),与缓解期CD患者相比,CD发作患者的群落结构与Kp的富集丰度相关(图1K)。
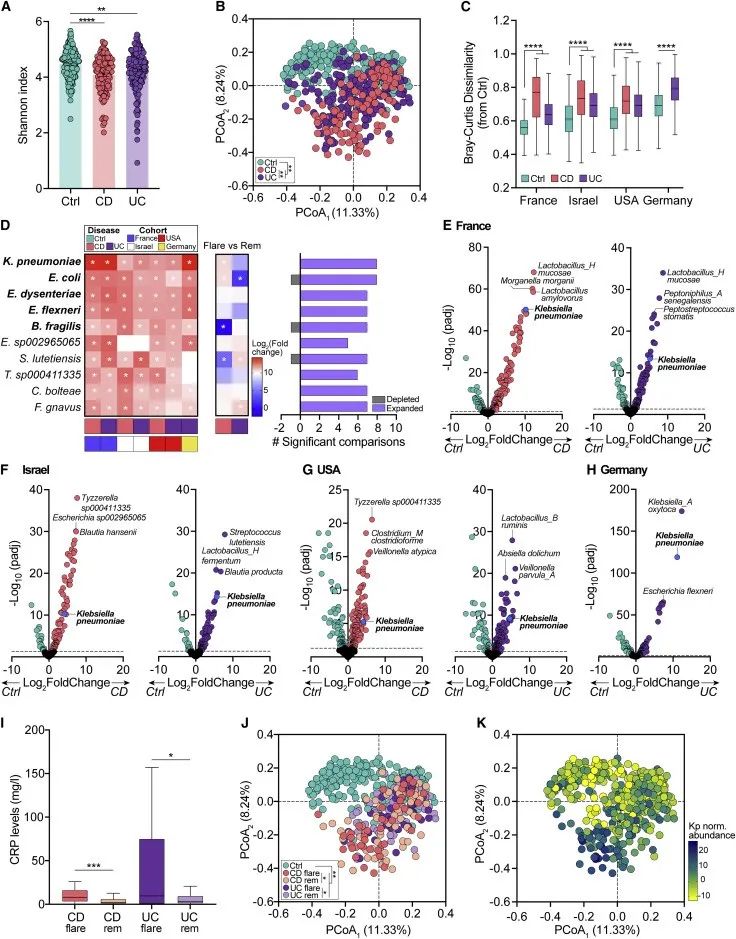
Figure 1. Geographically distinct IBD patients feature enriched intestinal K. pneumoniae
与健康对照组相比,CD和UC患者的抗性组α多样性(图2A)和差异抗性组组成(图2B)有所扩大,Kp丰度与整体抗性组谱显著相关(图2C)。同样,IBD患者具有更高的移动基因组α多样性(图2D)和差异性移动基因组谱(图2E),且与Kp相关(图2F)。遗传元件和菌群丰度的相关性分析揭示了肠杆菌科细菌与与疾病中高表达的差异性抗性基因和可移动元件之间的显著关联,其中一些与Kp密切相关(图2G)。在功能上,IBD患者与健康对照组的粪便微生物群聚集不同(图 2 H),这一特征也与Kp的差异丰度相关(图2I)。与对照相比,不同IBD亚型人群中的Kp菌株与氨基酸、核苷酸、甘露糖和果糖代谢相关的基因更为丰富(图 2 J)。

Figure 2. Functional analysis of K. pneumoniae in IBD patients
▼ 2. IBD-相关Kp的菌株特征
不同地区的IBD患者中,Kp的丰度较对照组显著增加(图3A)。研究者从NCBI下载了包括Kp-2H7在内的356个Kp菌株的基因组序列,构建单核苷酸变异(SNV)图谱,并定义了89个代表性Kp菌株。与缓解状态相比,Kp KSB1_4E(GenBank:GCA_002754835.1)菌株在所有 IBD 亚型及疾病发作期患者中显著丰富。该菌株与先前发现的Kp-2H7菌株聚集在同一进化枝中,被共同称为“IBD相关”或Kp2进化枝(图3C),MLST分析揭示该进化枝均属于ST323。
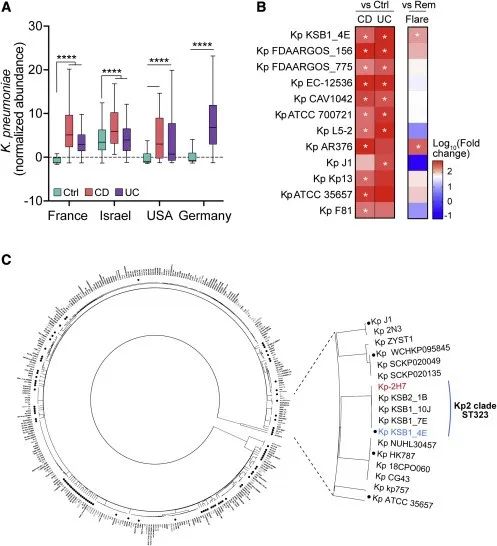
Figure 3. IBD patients feature an enriched intestinal Kp2 clade
▼ 3. IBD相关Kp临床分离株诱导小鼠结肠促炎反应
研究者将非Kp2和Kp2临床分离株分别接种到无菌野生型小鼠中(图4A),并测试不同菌株的定植和诱导促炎反应的能力,结果表明Kp菌株均能定植于小鼠肠道,并在结肠中差异性地诱导促炎症反应(图4B),Kp临床分离株与非Kp2参考菌株KTCT 2242相比,干扰素-γ和IL-17共表达显著增加(图4C)。
随后,研究者将11株Kp临床菌株混合菌群接种至GF Vert-X IL-10-eGFP报告小鼠构建定植模型,2周或4周后处死小鼠获得离体脾细胞,用单一菌株的Kp裂解物再刺激脾细胞,结果发现,Kp2临床分离株较非KP2菌株诱导更低的IL-10表达和分泌(图4E),Kp2菌株刺激的脾细胞检测到较高的 IFN-γ/IL-10 比率,呈现促炎反应(图4F)。
后续研究中,研究者选择三种最有可能诱导促炎反应的 Kp2 菌株定植于GF IL-10-/-小鼠两周(图4G),Kp2菌株均能诱导粪便脂质运载蛋白(图4H)和IFN-γ(图4I),且Kp2菌株诱导的促炎指标和肠道炎症损伤的组织病理学评分呈正相关(图4J-L)。
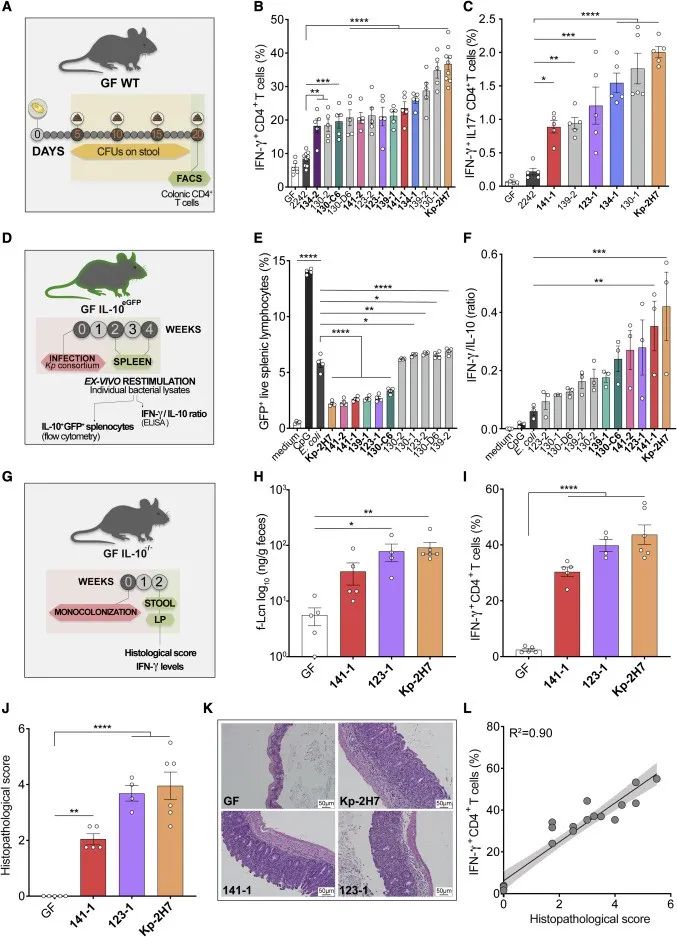
Figure 4. Intestinal colonization by clinical Kp2 isolates drives enhanced inflammation and tissue damage in mice.
▼ 4. 靶向Kp噬菌体组合的分离和选择
研究者针对Kp2菌株进行了一系列的噬菌体分离、鉴定和体内外验证实验后,获得8种噬菌体并组合成18种不同的三联/四联/五组噬菌体组合(图5A)。所有18 种噬菌体组合均包括噬菌体 MCoc5c(具有最广泛的宿主范围且对14株Kp2均有效)和噬菌体 8M-7(成功裂解对 MCoc5c 产生抗性的突变体)。体外验证试验以Kp-2H7 和两株Kp2临床分离株为实验菌株,五种噬菌体组合 3(D)、4(F)、4(G)、5(E)和5(F)证实体外有效继而进行体内测试(图5B-D)。体内实验结果(图5F-G)显示,Kp-2H7定植并用噬菌体4(F)、4(G)和5(E)处理组以及123-1 Kp2定植并用噬菌体5(E)和5(F)处理组的Kp负载降低最为明显。因此,由噬菌体 MCoc5c、8M-7、1.2-3s、KP2-5-1 和 PKP-55 组成的噬菌体组合5(E),能最大效率地减少人类IBD相关Kp2菌株的负载。
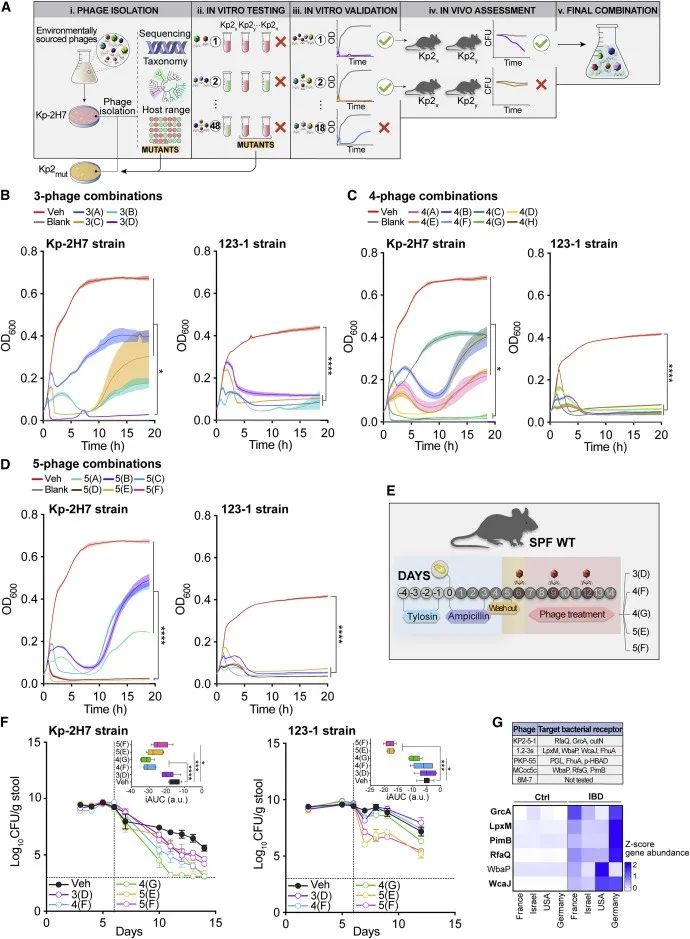
Figure 5. Selection and testing of Kp2-targeting bacteriophages
▼ 5. 噬菌体疗法可治疗Kp2诱导的结肠炎症
研究者继续评估在临床前IBD模型中减少Kp2负载和影响结肠炎症的功效(图6A-B),结果显示通过每周3次使用109 PFU/mL噬菌体组合5(E)可实现噬菌体最高效率的复制(图6A),同时可促进Kp2的最佳根除(图6B-D)。
随后,研究者利用口服右旋糖酐硫酸钠 (DSS) 诱导的急性 IBD 样自身炎症模型评估了噬菌体组合5(E)的疗效。结果表明,噬菌体处理组小鼠大肠粪便和粘膜中的细菌负荷持续降低,炎症指标和组织损伤明显改善(图6E-M)。
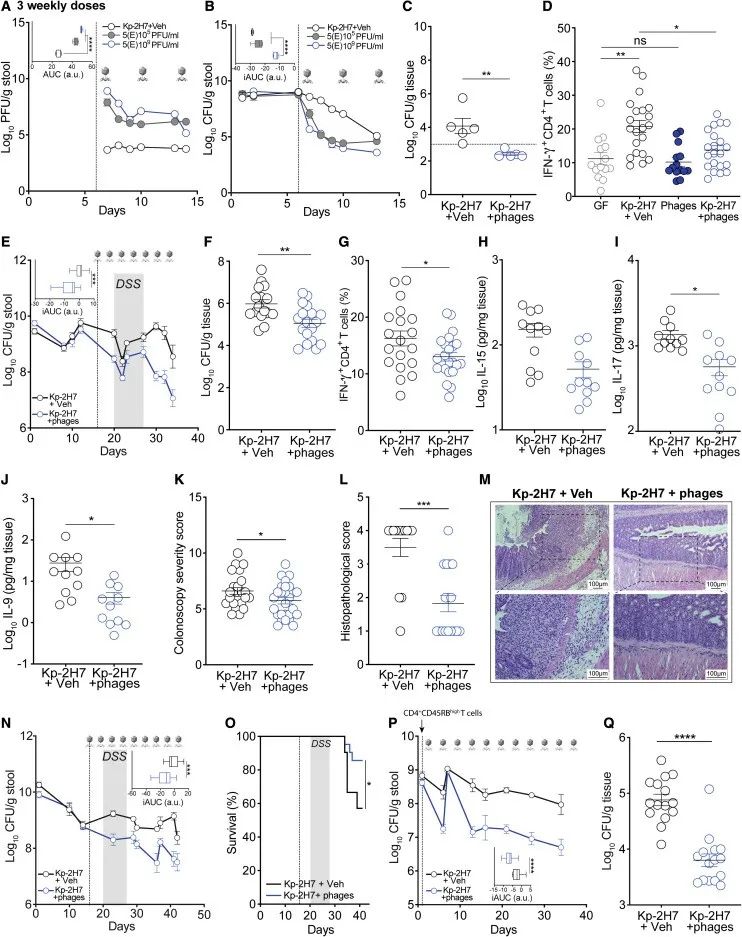
Figure 6. A phage combination is effective in ameliorating colitis in mice
▼ 6. Kp2 靶向噬菌体能在人类胃肠道中稳定存在
研究者评估了噬菌体组合5(E) 的两种噬菌体(1.2-3s和MCoc5c)在通过人类肠道微生物生态系统模拟器时的稳定性(图7A)。“进食”(低 pH)和“禁食”(高 pH)之间噬菌体活性存在显著差异,在低pH条件下时噬菌体会丧失部分活性,在较高的胃pH条件下,噬菌体稳定性更高(图7B),此外,两种噬菌体的活性在代表更远端肠道生态位(例如空肠、回肠以及近端和远端结肠)的其他腔室中的长时间孵育中保持稳定(图7B-7D )。
最后,研究者开展了一项临床试验(ClinicalTrials.gov:NCT04737876)以评估口服联合噬菌体后,两种噬菌体在健康人体胃肠道中的活力(图7 E)。试验结果表明,MCoc5c 和 1.2-3s 的总 PFU 中位数分别为 1.46 × 10 10和 1.08 × 10 9(图 7 F),且在第 4、5、6 天所有的受试者都检测到了噬菌体(图7G),证实了该制剂噬菌体的持久性。总的来说,口服两种Kp靶向噬菌体在健康成年人中是安全的,且耐受性良好。
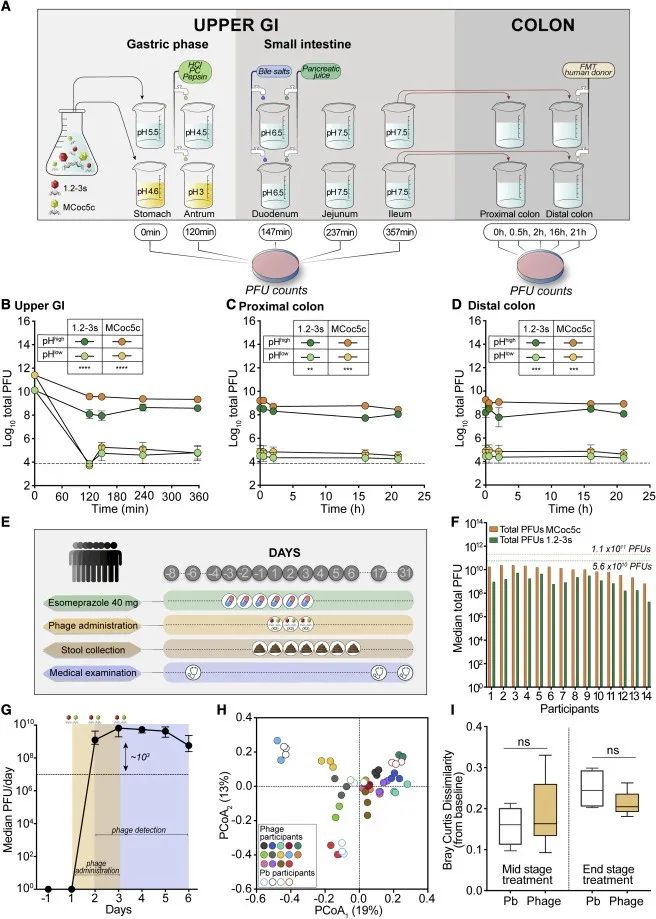
Figure 7. Orally administered phages persist and accumulate in the lower gut of healthy human volunteers
▼ 研究结论:
本研究揭示了四个不同国家的IBD患者肠道中Kp富集的现象,鉴定出了其中特定的Kp亚群(Kp2 clade),并证实该亚群与IBD患者的肠道炎症状态密切相关。将临床IBD相关Kp菌株转移到易患结肠炎的无菌小鼠体内可诱导小鼠的肠道炎症。针对Kp2菌株分离、筛选、设计出的五种噬菌体混合物,在小鼠肠道炎症模型上可有效抑制Kp,从而减轻炎症和疾病严重程度。人类肠道微生物生态系统模拟器和I期临床试验表明,噬菌体能在下肠道中保持活力,并具有较高的安全性,口服噬菌体联合治疗能在避免细菌产生耐药性的同时,有效抑制病原菌。该研究结果表明,噬菌体疗法可能成为调节肠道微生态平衡和治疗炎症性肠道疾病的一种有前景的方法,为未来的疾病治疗研究提供了新的思路的方法。
▲点击图片,关注2023京港年会

张丽玮
浙江大学医学院附属第二医院检验科
END
作者|张丽玮(浙江大学医学院附属第二医院)
审校|张嵘(浙江大学医学院附属第二医院)


