2018-12-02 16:53
作者 宁永忠
岁末天寒,万物蛰静。感染病领域却相反,热闹非凡。12月月初CID发布文章,IDSA官方声明不认可SSC2016指南,一时天下哗然、舆论沸腾。笔者细看原文,大旨可思!果然是IDSA,真知灼见、严谨求实。当然也有细节是吹毛求疵(比如微生物学部分),而有的后续证据补充,则事后诸葛、不必苛责。IDSA声明这一个炸弹我们先放在一旁。笔者这里给大家介绍另一篇文章,也引起一定的争议。国内认为是“颠覆概念”。
题目:MIC-based dose adjustment: facts and fables(基于MIC的剂量调整:事实和杜撰)。
作者:一作兼通讯作者是Johan W. Mouton,任职于荷兰Erasmus医学中心医学微生物学与感染病学部门。其他5位作者来自荷兰、西班牙、瑞典和澳大利亚。
著录:Mouton JW, Muller AE, Canton R, Giske CG,Kahlmeter G, Turnidge J. MIC-based dose adjustment: facts and fables. JAntimicrob Chemother. 2017 Dec 5. doi: 10.1093/jac/dkx427. [Epub ahead ofprint]
摘要:近年来,若干出版文献描述了基于抗微生物药物MIC值进行的抗生素个体化治疗优化的过程。多数方法包括:治疗药物监测(therapeutic drug monitoring,TDM),单一MIC值加相关PK/PD参数来优化抗微生物药物暴露剂量、优化抗细菌效果。然而,使用单一MIC值是不恰当的。首先,常规实验室测试MIC的准确性(accuracy,亦即精确性)不够,MIC试验内在的方法学变异性(inherent assay variation)导致结果不足以指导剂量调整。第二,无论使用何种方法,必须考虑MIC的变异。如果基于TDM和MIC来调整剂量,必须考虑MIC以防止剂量偏低。本文将呈现出这些难题,并给出临床实践时的一些方式。
正文的关键信息(建议阅读原文全文):
1.MIC代表了什么?此处作者提到这是体外的标准化实验。而实际感染部位,细菌浓度会比实验高,细菌生长也不同于体内生长。
2.MIC的准确性(accuracy)意味着什么?作者提到,实验室内重复实验有0.3-0.5 个log2的变异。而实验室间是0.5-1个。由此国际标准中以1个2倍稀释为实验变异。也就是说A结果与B结果相差一倍,可以认为结果一样。
3.同种不同株的生物学变异。此处提到了野生株(wild type,WT)、流行病学界值(epidemiological cut-off,ECOFF)
4.MIC结果的变异:来自生物学变异、方法学变异(assay variation),后者为主。
5.MIC和PK/PD的关系。具体内容是临床细菌学常识(PK/PD折点的来源),笔者不必展开。此节是本文的基轴,因为从这里开始,文章逐渐讨论了基于MIC的剂量调整,而其理论依据是PK/PD。作者认为,对某一种疾病整体,药效学达标是准确的;而对于个体,这将不再准确。
6.MIC、TDM和剂量调整。作者提到,近年来TDM大量应用,数篇文献揭示出特定人群很难达到PK/PD目标——主要原因是清除率增加。作者认为,基于上述MIC结果的变异,根据MIC结果进行药物调整会导致药物剂量偏低。因此建议,即使MIC只有2倍的变异,PK浓度也应该有4倍变化,因为PK/PD目标(如AUC/MIC)是4倍变化。
7.基于MIC的实践指南(practice guidance)
首要的(注意此处是first,不是firstly),要以分布(distribution)的观点来考虑MIC。原文给出了图示如下,一目了然。笔者体会,您拿到一个具体MIC结果时,要放在一个分布的时空背景(图示)中理解——这样方法学变异、生物学变异、患者体内的特有变化、实际操作波动等,都会涵容并包、不出方外。
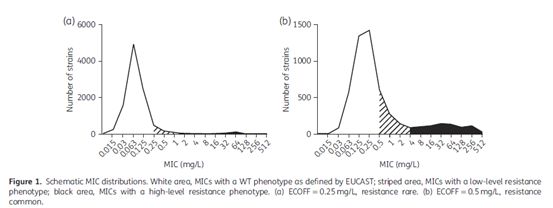
作者将MIC分布分成三种情况:WT(空白)、低水平耐药(斜线)、高水平耐药(黑色)。并以此为基础,讨论了下列4种情景。
7a.结果在WT区(空白区)。此时意味着ECOFF可以作为PK/PD目标。
7b.结果刚刚超过ECOFF(斜线区左侧)。此时基于实际操作的波动、方法学变异等因素,建议两个2倍数值为PK/PD个体化目标。作者强调:这没有共识,目的是扩大安全边界。
7c.结果肯定不在WT范围,也远远超过临床折点。此时没有机会调整药物浓度,基于MIC的治疗不再是一个选择。
7d.这是前两种情况的交集。左图分布不太可能。右图分布有可能。就是一个低水平耐药菌,其测试MIC落在WT范围内(边缘)。尚不确知具体的比例,具体药物与菌种对应也各不相同。作者强调,这是需要进一步研究的地方。
基于上述分析,作者汇总建议形成表格如下。
表 不同情况下达标MIC的建议性解释
MIC | 达标解释 |
在WT区域,≤ ECOFF | ECOFF |
> ECOFF | MIC基础上提高2个稀释度a |
a,实际提高倍数可以高于或低于2。这取决于实验室能力、具体药物菌种组合分布。
笔者按:
1.全文学习后,笔者觉得并不存在“颠覆概念”的观点。只是对一贯的专业思路的反思、细化。
2.这是几位西方作者的专家观点。专家观点在西医循证医学体系中,是证据级别最低的证据,建议仅供参考。所以,不必夸大。
3.原文讨论充分、逻辑明确、观点清晰,所以结论值得重视。当然也需要进一步获得客观证据来证实或证伪。
4.结论不是“不能依赖MIC来调节药物剂量”。而是要作精细化分析,因应具体情况不同而有具体差异。
5.对于国内现实,因为TDM没有普遍展开,所以基于MIC精细调整药物剂量,可能有个别患者有此经历;但作为整体性的、系统性的临床行为,就笔者所知还是空白。因此,就国内普遍情况,基于MIC精细化调整剂量还不是现实。换句话说,西方专业领域反思,是既证之后(他们普遍TDM的药物也不多,国内是一个都没有);而我们的现实,尚在未证之先。他们是彼岸回首,我们是此岸遥望。当然类似反思对我们未来会大有助益。退一步讲,国内大多数抗生素的使用还没有微生物学导向,感染性疾病诊治防控还没有微生物学思维,所以类似基于MIC的剂量调整,只是水中望月——真的很美......
投稿人:宁永忠 北京市垂杨柳医院
责任编辑:曾吉 杨青



