2021-08-06 18:52
作者 王启

京港感染论坛
早诊快诊,助力精准防治
2021年美国临床和实验室标准化协会(Clinical and Laboratory Standards Institute,CLSI)M100 S31文件中修订了除金黄色葡萄球菌,路邓葡萄球菌以外的葡萄球菌属对苯唑西林的药敏折点。本文就该折点修订依据做了简要阐述。
凝固酶阴性葡萄球菌是人体皮肤和粘膜表面的正常菌群,也是临床重要的机会致病菌,主要与导管、植入物及器械相关的感染有关[1]。目前,凝固酶阴性的葡萄球菌中已被确认和描述的有79个种或亚种(https://lpsn.dsmz.de/)。传统的通过形态学和生化反应谱鉴定凝固酶阴性葡萄球菌到具体的种或亚种较为困难。但随着基质辅助激光解吸电离-飞行时间质谱(Matrix assisted laser desorption ionization time of flight mass spectrometry,MALDI-TOF MS)技术在临床微生物实验室的普及,凝固酶阴性葡萄球菌的鉴定在临床上越来越细化。在种属水平上的准确鉴定,提高了实验室对特定菌种临床意义的理解。但是,检测凝固酶阴性葡萄球菌mecA或mecC基因介导的耐药性目前还存在挑战。从1986年起,NCCLS(CLSI)建立了葡萄球菌属对甲氧西林、苯唑西林等青霉素酶稳定青霉素的药敏折点以来,为适应临床抗菌药物的合理使用,CLSI对其进行了多次评估和修订(表1)。
表1.历年来CLSI对葡萄球菌苯唑西林耐药性检测的修订

表2.除金黄色葡萄球菌以外的葡萄球菌属对苯唑西林的折点(CLSI)[2,3]
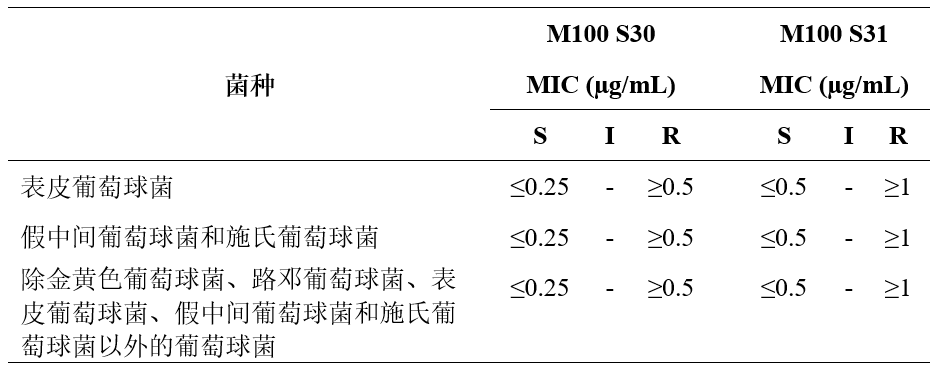
CLSI在2021年M100-S31中再次修订了金黄色葡萄球菌以外的葡萄球菌对苯唑西林的折点,见表2。苯唑西林敏感折点提高到了≤0.5µg/mL,修订依据较为严格。Romney M.Humphries等人对2014年~2018年多地区不同标本来源收集的198株凝固酶阴性葡萄球菌进行的苯唑西林药敏试验的再评估[4],结合之前已经发表的研究结果中的菌株共计1052株凝固酶阴性葡萄球菌[5-7]。评估结果如表3和图1所示,以mecA基因的PCR结果阳性为“金标准”,检测苯唑西林耐药时,使用“旧折点”(M100 S30),全部菌株的极重大错误(Very major errors,VMEs)率为1.2%(6/490株mecA基因阳性),重大错误(Major errors,MEs)率为4.4%(25/562株mecA基因阴性);其中沃氏葡萄球菌ME率为21.3%(16/75株mecA基因阴性)。使用“新折点”(M100 S31),全部菌株的VMEs率为1.6%(8/490株mecA基因阳性),MEs率为0.89%(5/562株mecA基因阴性)[4]。图1中有较多数量的人葡萄球菌和沃氏葡萄菌MIC值为0.5µg/mL,这也是使用旧折点判定结果时产生较高比例MEs的主要原因。在我国目前临床主流自动化药敏试验板条中,多数厂商所能够报告的苯唑西林MIC范围在0.25~4µg/mL之间,能够支持折点修改后的结果判定。
表3.苯唑西林的新折点(M100 S31)和旧折点(M100 S30)对凝固酶阴性葡萄球菌药敏结果分析[4]
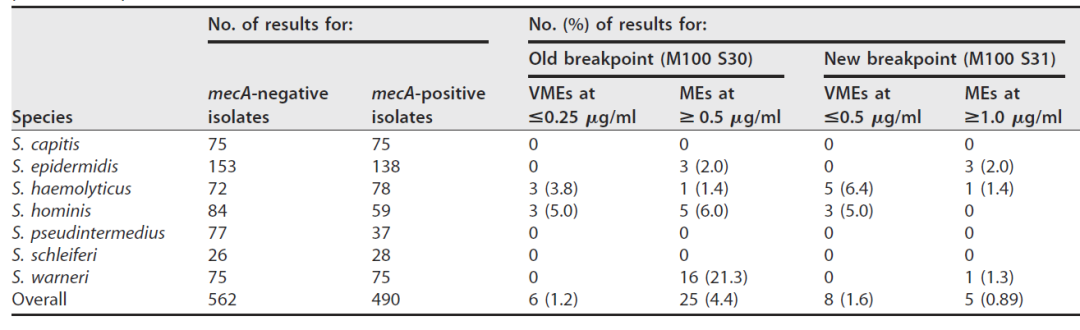
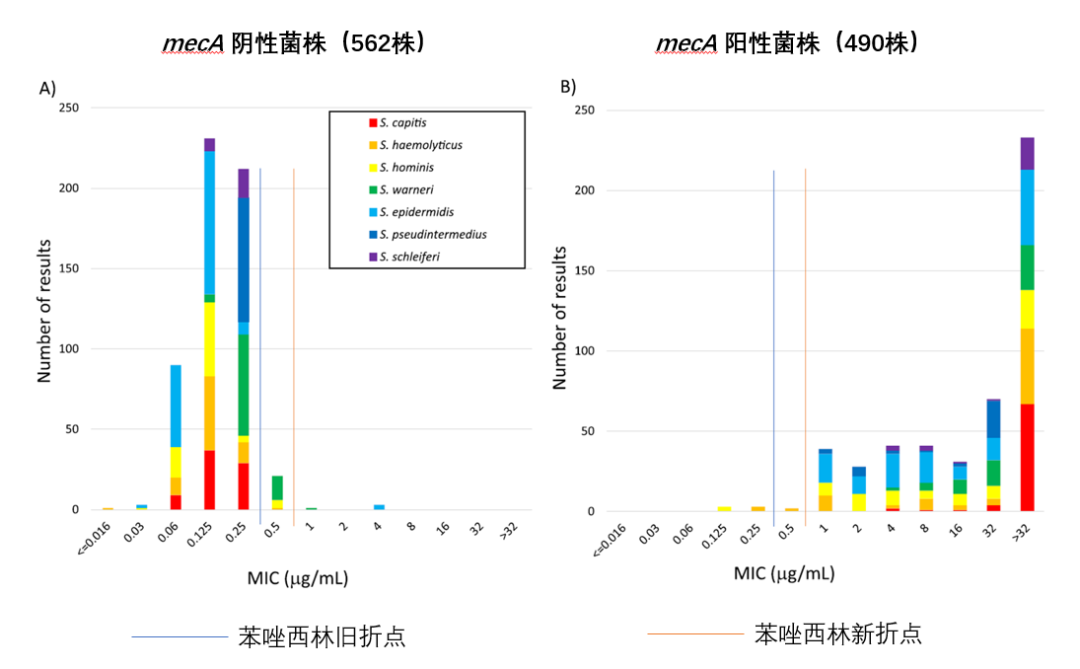
图1. A)mecA基因阴性的凝固酶阴性葡萄球菌苯唑西林的MIC值分布;B)mecA基因阳性的凝固酶阴性葡萄球菌苯唑西林的MIC值分布[4]
参考文献(上下滑动)
[1] Becker K, Heilmann C, Peters G. Coagulase-negative staphylococci. Clin Microbiol Rev 2014; 27(4): 870-926.
[2] CLSI.Performance standards for antimicrobial susceptibility testing. 31sted. CLSI supplement M100. Wayne, PA: Clinical and Laboratory Standards Institute; 2021.
[3] CLSI.Performance standards for antimicrobial susceptibility testing. 30thed. CLSI supplement M100. Wayne, PA: Clinical and Laboratory Standards Institute; 2020.
[4] Humphries RM, Magnano P, Burnham CA, et al. Evaluation of surrogate tests forthe presence of mecA-mediated methicillin resistance in Staphylococcus capitis,Staphylococcus haemolyticus,Staphylococcus hominis,and Staphylococcus warneri.J Clin Microbiol 2020; 59(1): e02290-20.
[5] Wu MT, Burnham CA, Westblade LF, et al. Evaluation of oxacillin and cefoxitin disk and MIC breakpoints for prediction of methicillin resistance in human and veterinary isolates of Staphylococcus intermedius group. J Clin Microbiol 2016; 54(3): 535-542.
[6] Huse HK, Miller SA, Chandrasekaran S, et al. Evaluation of oxacillin and cefoxitin disk diffusion and MIC breakpoints established by the Clinical and Laboratory Standards Institute for detection ofmecA-mediatedoxacillin resistance in Staphylococcusschleiferi.J Clin Microbiol 2018; 56(2): e01653-17.
[7] NaccacheSN, Callan K, Burnham CA, et al. Evaluation of oxacillin and cefoxitin disk diffusion and microbroth dilution methods fordetecting mecA-mediated beta-lactam resistance in contemporary Staphylococcus epidermidis Isolates.J Clin Microbiol 2019; 57(12): e00961-19.
作者简介

王启
王启,副主任技师,毕业于北京大学医学部,临床检验诊断学专业。2009年至今工作于北京大学人民医院检验科,师从北京大学人民医院检验科王辉教授。主要从事细菌耐药监测,感染性疾病的实验室诊断工作。主要研究方向为碳青霉烯耐药的肠杆菌科细菌流行病学与耐药机制。负责具体实施中国美罗培南敏感性监测(CMSS)工作。主持国家自然科学基金1项,北京大学人民医院院内发展基金1项。以第一作者在感染及临床微生物领域Clinical Infectious Disease, Antimicrobial Agents and Chemotherapy等杂志上发表论文多篇。
END
作者|王启
审校|王晓娟



